這個條目來自axispharm
谷氨酰胺代謝在癌癥生長、能量產生和生物合成中起著關鍵作用。自1935年漢斯·克雷布斯首次描述三羧酸(TCA)循環以來,研究強調了谷氨酰胺在正常細胞和癌細胞中的重要性。今天,在癌癥治療中靶向谷氨酰胺途徑顯示出有希望的潛力。該指南解釋了谷氨酰胺的影響,它在自噬和活性氧中的作用,針對它的策略,以及未來治療的考慮。
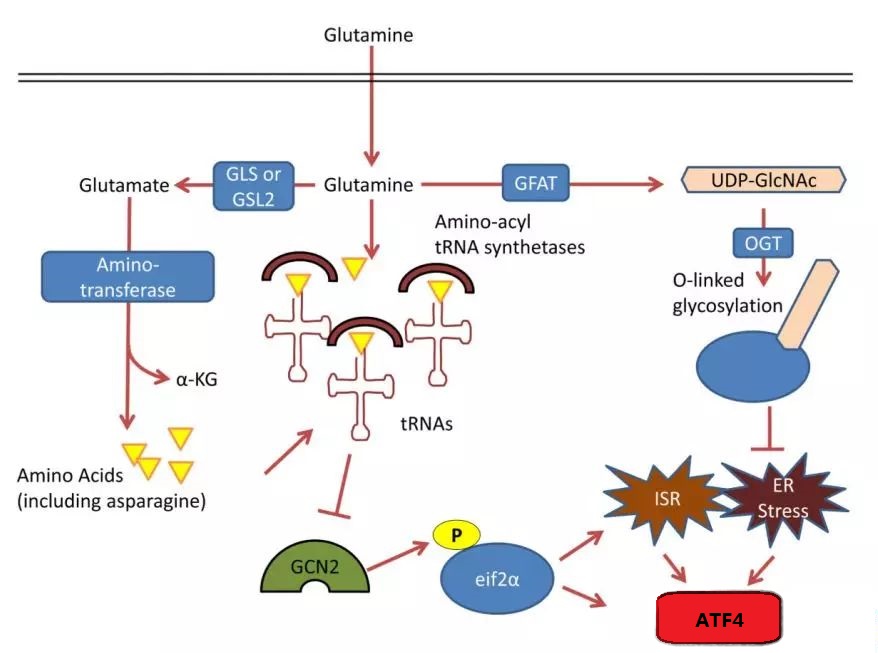
核酸、脂質和蛋白質中谷氨酰胺的合成
1. 癌細胞中的谷氨酰胺代謝
癌細胞嚴重依賴谷氨酰胺:
- 能源生產:谷氨酰胺為TCA循環提供燃料,轉化為α-酮戊二酸提供能量。
- 生物合成:它為構建核苷酸、脂質和蛋白質提供碳和氮。
- 代謝靈活性:當營養物質缺乏時,癌細胞會轉而使用谷氨酰胺作為能量來源。
癌細胞使用幾種策略來獲得谷氨酰胺:
- 高攝取量:它們通過SLC1A5這樣的轉運蛋白吸收谷氨酰胺。
- 營養清除:在應激狀態下,細胞分解內部成分或吞噬蛋白質以獲得谷氨酰胺。
2. 谷氨酰胺在生物合成中的作用
-
核酸合成
- 谷氨酰胺為制造嘌呤和嘧啶提供氮。沒有它,癌細胞可能會停止分裂。
- 它激活mTOR途徑,刺激參與核苷酸生產的酶。
-
脂質合成
- 谷氨酰胺衍生的α-酮戊二酸轉化為乙酰輔酶a,支持脂質形成。
-
蛋白質合成
- 谷氨酰胺為氨基酸提供氮,并幫助蛋白質折疊。低水平會導致蛋白質壓力。
3. 谷氨酰胺代謝途徑
-
TCA循環和IDH2
- 在TCA循環中,谷氨酰胺衍生的α-酮戊二酸轉化為異檸檬酸和檸檬酸。酶IDH2有助于這一過程,促進能量產生。
- IDH2的突變可以破壞谷氨酰胺代謝,影響癌癥生長。
-
谷胱甘肽途徑
- 谷氨酰胺代謝產生谷氨酸,是谷胱甘肽的前體。這種抗氧化劑可以中和有害的活性氧(ROS)。
- 通過谷氨酰胺代謝產生的NADPH支持谷胱甘肽再生,有助于控制活性氧水平。
4. 谷氨酰胺和自噬在癌癥研究中的作用
谷氨酰胺在自噬中起著重要作用,自噬是細胞分解自身成分獲取營養的過程:
- 提高癌癥存活率:當營養物質不足時,谷氨酰胺支持自噬,讓癌細胞自我維持。
- 在腫瘤生長中的雙重作用:自噬既可以幫助腫瘤生長,也可以阻礙腫瘤生長。雖然它可以減少氧化壓力,防止染色體不穩定,但它也有助于癌細胞在壓力下生存。
- 與壓力通路相互作用:谷氨酰胺通過mTOR和GCN2等途徑影響自噬,促進營養攝入和管理細胞應激。
5. 谷氨酰胺和活性氧在癌癥研究中的作用
谷氨酰胺和活性氧
癌細胞需要控制活性氧水平以避免損傷:
- 中等活性氧水平:低至中等水平通過細胞分裂信號促進細胞生長。
- 高活性氧水平:過多的ROS會損傷細胞,導致細胞死亡。癌細胞需要小心平衡活性氧以避免傷害。
- 用谷氨酰胺調節活性氧:通過代謝,谷氨酰胺生成谷胱甘肽和NADPH。兩者對于中和活性氧和保護細胞免受損傷都是至關重要的。
- 影響腫瘤微環境:谷氨酰胺衍生的代謝物有助于控制腫瘤微環境中的ROS,幫助癌細胞適應和存活。
6. 谷氨酰胺和T細胞
谷氨酰胺不僅對癌細胞重要。它還刺激免疫細胞,尤其是T細胞:
- 早期激活:在活化過程中,T細胞需要谷氨酰胺才能快速生長和分裂。它提供能量和基本的建筑材料。
- t細胞分化:谷氨酰胺影響CD4+ T細胞如何發育成不同的亞型,從而影響免疫反應。
7. 靶向谷氨酰胺代謝的策略
擾亂谷氨酰胺代謝會削弱癌細胞:
- 谷氨酰胺酶抑制劑(如CB-839):這些藥物阻斷谷氨酰胺酶,阻止谷氨酰胺轉化為谷氨酸。
- 轉運蛋白抑制劑:靶向谷氨酰胺轉運蛋白如SLC1A5會減少谷氨酰胺的攝取,剝奪細胞的營養。
- 聯合治療:谷氨酰胺抑制劑與化療、免疫療法或IDH2抑制劑聯合使用可提高療效。
8. 谷氨酰胺靶向治療的關鍵考慮
谷氨酰胺酶抑制劑的臨床應用
-
代謝靈活性
- 癌細胞通過轉換代謝途徑來適應營養變化。了解這些變化可以發現新的治療方法。
-
腫瘤微環境
- 缺氧和酸度等因素會影響細胞如何利用谷氨酰胺。增加改變腫瘤環境的療法可能會提高療效。
-
谷氨酰胺成癮
- 一些腫瘤嚴重依賴谷氨酰胺。將谷氨酰胺靶向治療與癌基因抑制劑結合可能產生合成致死性。
-
靶向谷氨酰胺轉運蛋白
- 抑制SLC1A5等轉運蛋白會切斷谷氨酰胺的供應,進一步限制生長。
-
免疫代謝和T細胞活化
- 谷氨酰胺在活化過程中幫助T細胞,并影響它們的功能。在免疫治療的同時使用谷氨酰胺靶向治療可以增強抗癌效果。
-
谷氨酰胺代謝的生物標記
- 跟蹤谷氨酰胺相關標記物有助于個性化治療。
-
組合方法
- 谷氨酰胺酶抑制劑與標準療法相結合可能會提高療效。這種策略還可以增加癌細胞對某些藥物的敏感性。
-
平衡治療和毒性
- GLS抑制劑可以選擇性地靶向癌細胞,將對正常細胞的傷害降至最低。
-
飲食和谷氨酰胺攝入
- 減少飲食中的谷氨酰胺可能會增強治療效果。然而,飲食、新陳代謝和治療之間的關系是復雜的。
-
轉移預防
- 靶向谷氨酰胺代謝可以通過限制細胞的適應能力來降低癌癥擴散的風險。
9. 谷氨酰胺酶抑制劑的臨床進展
谷氨酰胺酶抑制劑選擇性地靶向癌細胞中過度活躍的GLS,放過正常細胞中的GLS2:
- 阻斷上皮-間質轉化:這些抑制劑有助于防止支持癌癥擴散的EMT。
- 結合免疫療法:因為谷氨酰胺為T細胞提供燃料,將抑制劑與免疫治療配對可以增強抗癌效果。
10. 未來方向
- 新藥篩選:自動化技術可以幫助找到更好的谷氨酰胺酶抑制劑。
- 精確醫學:基于腫瘤代謝概況的定制治療可以改善結果。
- 超越新陳代謝的探索:谷氨酰胺可能影響基因調節,提供新的治療可能性。
11. 結論
谷氨酰胺代謝在癌細胞和免疫細胞如T細胞中起著至關重要的作用。它影響自噬和活性氧調節等過程,影響癌癥的生長和存活。針對這一途徑為癌癥治療提供了一個有希望的策略,特別是與其他治療方法結合使用。隨著研究的進展,更有效的方法將會出現。



